Методология флоуметрии, Выпуск 5, 2001 г. стр.87-99.
Влияние корригирующей антиоксидантной терапии на микроциркуляцию при панкреонекрозе
Ю.С.Винник, Д.В.Черданцев, О.В.Первова
Красноярская государственная медицинская академия
При остром панкреатите в поджелудочной железе (ПЖ) происходят нарушения микроциркуляции, приводящие к возникновению гипоксии, ацидозу и фокальной энергетической недостаточности. В этих условиях возможна активизация процессов перекисного окисления липидов (ПОЛ) в панкреатоцитах, сопровождающаяся повреждением мембран, активацией ферментов внутри клетки и «самоперевариванием» ткани ПЖ [8].
Активация свободнорадикальных процессов, сопровождающаяся депрессией естественных антиоксидантных систем (АОС), расценивается как окислительный стресс [1, 2, 4, 5].
Система микроциркуляции - один из первых и наиболее чувствительных уровней реализации патологических эффектов окислительного стресса. Микроциркуляторные нарушения носят генерализованный характер, имеют определенную стадийность и, как правило, детерминированы формой панкреатита и тяжестью деструктивных изменений в железе [3, 6, 7, 9, 10].
До недавнего времени отсутствие объективных прямых методов исследования микроциркуляции не давало возможности оценить наличие взаимосвязи между окислительным стрессом и тяжестью системных микроциркуляторных нарушений, а также исследовать влияние различных методов антиоксидантной терапии на систему микроциркуляции.
В клинике общей хирургии Красноярской государственной медицинской академии разработана оригинальная методика антиоксидантной терапии при панкреонекрозе, основанная на сочетанном применении чрескожной инфракрасной (ИК) лазеротерапии и озонотерапии.
Исследование эффективности сочетанного применения внутривенного введения озонированного физиологического раствора (ОФР) и чрескожной ИК лазеротерапии проведено у 12 больных с различными формами деструктивного панкреатита. Контрольную группу составили 22 больных панкреонекрозом, которые в послеоперационном периоде получали традиционную терапию.
Забор крови для исследования производили при поступлении и на 2, 4, 6, 8, 10, 12, 14, 18, 22, 28, 38 сутки госпитализации. Биохимическое исследование включало следующие параметры: определение билирубина, мочевины и амилазы сыворотки крови. Для диагностики интегральной токсичности крови определяли люциферазный индекс (ЛИ). Интенсивность процессов ПОЛ оценивали по накоплению конечного продукта ПОЛ – малонового диальдегида (МДА). Исследование показателей состояния антиоксидантной системы включало следующие параметры: определение содержания глутатиона (ГНS) и его ферментов его метаболизма – глутатионредуктазы (ГР), глутатион-S-трансферазы (ГSТ), глутатионпероксидазы (ГП) в эритроцитах; в плазме определяли содержание церулоплазмина (Цп),
Периферическую микроциркуляцию оценивали методом лазерной допплеровской флоуметрии (ЛДФ) с помощью аппарата BLF-21 американской фирмы Transonic Systems inc.
Начиная с первых суток после операции, ежедневно один раз в день в течение 12-13 суток поводили сеансы чрескожной лазеротерапии в дозе 315 мДж/см2. Одновременно проводилась озонотерапия путем внутривенного введения 400 мл ОФР с концентрацией озона 6 мг/л, один раз в трое суток.
Анализ клинико-лабораторных показателей выявил следующие закономерности. Начиная с 4-х суток, наблюдалось выраженное снижение концентрации МДА и ЛИ, причем значения этих показателей были достоверно ниже исходного и контрольного уровней и составили, в среднем, соответственно 9,65±0,64 мкмоль/л (P<0,05) и 0,32±0,05 у.е. (P<0,05). В эти же сроки достоверно снижался уровень амилазы, мочевины, билирубина крови. Тенденция к уменьшению значений показателей панкреатогенной токсемии и активности процессов ПОЛ прослеживалась до 8-х суток.
В дальнейшем, наблюдалось постепенное возрастание концентрации МДА, мочевины, значений ЛИ, амилазы крови. Пик наблюдаемой активации воспалительного процесса в этой группе больных регистрировался на 14-е сутки. Затем, вплоть до окончания наблюдения, происходило уменьшение величины регистрируемых параметров.
На фоне сочетанного применения лазеротерапии и внутривенных инфузий ОФР происходило достоверное увеличение показателей активности внутриклеточного звена антиоксидантной системы, по сравнению с исходным уровнем, уже на 4-е сутки. В эти же сроки после проведения очередного сеанса сочетанной терапии исследуемые параметры достоверно превышали уровень контрольных значений и показатели до лечения, что свидетельствует о раннем стимулирующем воздействии метода на систему антиоксидантной защиты.
Тенденция к выраженному повышению концентрации клеточного восстановленного глутатиона и ферментов глутатионовой АОС наблюдалась на протяжении последующих 8-и суток. Значения их были следующими: для ГsН 6,86±0,51 мкмоль/гHb (P<0,05), для ГП 152,1±2,16 мкмоль/мин/гHb (P<0,05), для ГР и ГSТ соответственно 4,03±0,62 мкмоль/мин/гHb (P<0,05) и 5,03±1,03 ммоль/мин/гHb (P<0,05).
В период с 14 по 18 сутки происходило умеренное снижение показателей активности внутриклеточной глутатионовой АОС. Минимальные значения глутатиона были равны 4,04±0,45 мкмоль/гHb (P<0,05), что на 52,5% выше концентрации восстановленного глутатиона в контрольной группе. Подобная динамика наблюдалась при исследовании активности ферментов, входящих в глутатионовую систему - ГП, ГР, ГSТ.
После спада активности внутриклеточной антиоксидантной системы, совпадающего с активацией свободнорадикального окисления, динамика изменений АОС в исследуемой группе больных принципиально отличалась от таковой у больных, получавших в послеоперационном периоде традиционную терапию. В исследуемой группе отмечено повышение концентрации восстановленного глутатиона на протяжении всего периода наблюдения, которая к моменту выписки достигала уровня 14,08±2,01 мкмоль/гHb (P<0,05), что на 46% выше контрольных значений.
Кроме того, на фоне корригирующей антиоксидантной терапии зарегистрировано увеличение активности ферментов глутатионовой АОС. К концу наблюдения активность ГП, ГР и ГSТ составила соответственно 112,4±2,02 мкмоль/мин/гHb (P<0,05), 3,64±0,47 мкмоль/мин/гHb (P<0,05) и 4,13±1,01 ммоль/мин/гHb (P<0,05), которые превышали значения контрольной группы соответственно на 105,3%, 37,4% и 34,5%.
Таким образом, динамика изменения концентрации восстановленного глутатиона и активности ферментов глутатионовой антиоксидантной защиты у больных с деструктивным панкреатитом на фоне сочетанного применения лазеротерапии и озонотерапии свидетельствует о выраженном стимулирующем влиянии метода на внутриклеточную систему АОС.
При исследовании реакции компонентов плазменной антиоксидантной защиты на сочетанную терапию выявлены следующие закономерности. Динамика активности глутатионпероксидазы имела волнообразное течение, что выражалось в возрастании показателя в течение первых 8-и суток лечения до 10,64±0,52 мкмоль/мин*л плазмы (P<0,05), с последующим постепенным снижением активности внеклеточной ГП, которая к концу наблюдения составляла 7,94±2,25 мкмоль/мин*л плазмы (P<0,05), что на 53% выше значений контрольной группы.
При определении концентрации церулоплазмина в исследуемой группе, начиная с 6-х суток лечения было выявлено достоверное возрастание последней, и к окончанию наблюдения уровень Цп достигал 21,23±3,01 мг% (P<0,05), что на 37,7% выше концентрации этого белка в контрольной группе.
У больных на фоне сочетанной корригирующей терапии наблюдалась выраженная активация микроциркуляции в конъюнктиве, в коже передней брюшной стенки и верхней конечности (рис. 8.1.). Во всех точках регистрации на 4 сутки наблюдения цифры периферического кровотока были достоверно выше по сравнению с показателями до лечения (табл. 8.1.). В области передней брюшной стенки и конъюнктивы – показатели ЛДФ превышали исходные значения на 25,3% и 11% соответственно.
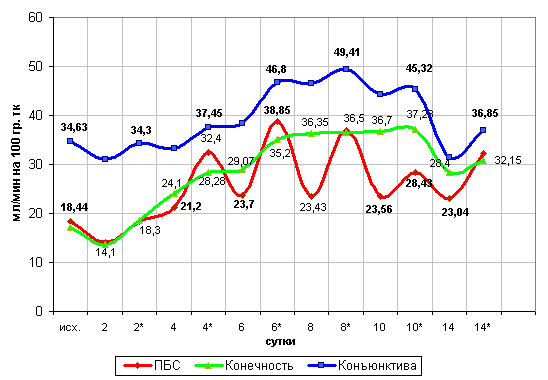
Рисунок 8.1. Сравнительная динамика периферической микроциркуляции на фоне сочетанной лазеро- и озонотерапии у больных панкреонекрозом.
В дальнейшем, тенденция к возрастанию уровня периферического микрокровотока прослеживалась до 8-х суток наблюдения. На 8-е сутки значения, зарегистрированные после лечения, были достоверно выше в сравнении с показателями до лечения во всех исследуемых областях и составили для передней брюшной стенки - 36,86±2,24 мл/мин на 100 гр. ткани (P<0,05), для верхней конечности - 36,5±3,2 мл/мин на 100 гр. ткани (P<0,05) и для конъюнктивы - 49,41±2,43 мл/мин на 100 гр. ткани (P<0,05).
В последующем было отмечено некоторое уменьшение интенсивности периферического микрокровотока. На 14-е сутки наблюдения цифры перфузии кожи передней брюшной стенки в области левого мезогастрия составили 32,15±2,32 мл/мин на 100 гр. ткани (P<0,05), уровень микроциркуляции конъюнктивы был равен 36,85±3,75 мл/мин на 100 гр. ткани (P<0,05), а верхней конечности - 30,91±1,54 мл/мин на 100 гр. ткани (P<0,05). К окончанию наблюдения уровень перфузии тканей соответствовал нормальным значениям.
Таблица 8.1. Динамика показателей периферической микроциркуляции у больных панкреонекрозом на фоне сочетанной лазеро- и озонотерпии.
| Сутки |
Перфузия
(мл/мин на 100 гр. тк.)
|
||
|
ПБС
|
Конечность
|
Конъюнктива
|
|
| Исходные (n=12) |
18,44±4,3
|
17,1±2,1
|
34,63±3,51
|
| 2 до лечения (n=12) |
14,1±1,411
|
13,73±0,631
|
31,1±2,22
|
| 2 после лечения (n=12) |
18,3±2,311
|
18,6±1,71
|
34,3±1,2
|
| 4 до лечения (n=11) |
21,2±1,351
|
24,1±2,811
|
33,34±1,56
|
| 4 после лечения (n=11) |
32,4±2,51123
|
28,28±2,5912
|
37,45±1,3512
|
| 6 до лечения (n=11) |
23,7±1,6312
|
29,07±2,061
|
38,4±1,021
|
| 6 после лечения (n=11) |
38,85±2,50123
|
35,2±2,26123
|
46,8±2,33123
|
| 8 до лечения (n=11) |
23,43±2,071
|
36,35±1,6112
|
46,62±1,111
|
| 8 после лечения (n=11) |
36,02±2,24123
|
36,52±3,212
|
49,41±1,43123
|
| 10 до лечения (n=11) |
23,56±2,0112
|
36,7±2,0612
|
44,31±2,43
|
| 10 после лечения (n=11) |
28,43±1,6612
|
37,23±2,1512
|
45,32±2,351
|
| 14 до лечения (n=11) |
27,04±1,2112
|
28,4±2,4212
|
31,51±1,141
|
| 14 после лечения (n=11) |
32,15±2,3212
|
30,91±1,5412
|
36,85±1,7512
|
Примечание: 1- достоверность по сравнению с исходными данными при P<0,05.
2 - достоверность по сравнению с показателями контрольной группы при P<0,05.
3 - достоверность по сравнению с показателями, регистрируемыми до лечения при P<0,05.
Высокие цифры показателей микроциркуляции по сравнению с исходными и контрольными значениями свидетельствуют об улучшении кровоснабжения тканей, что способствует снижению степени гипоксических нарушений в ПЖ, стабилизации клеточных энергетических процессов и системы антиоксидантной защиты.
Более благоприятное состояние периферической микроциркуляции в исследуемой группе, способствовало развитию менее выраженных деструктивных изменений в поджелудочной железе по сравнению с контрольной. Это в известной степени способствует снижению количества осложнений панкреонекроза, таких как абсцесс сальниковой сумки, гнойный панкреатит, аррозивное кровотечение, образование внутренних и наружных дигестивных свищей, эвентерация и т.п.
Анализ частоты развития перечисленных осложнений, наблюдаемых в послеоперационном периоде, выявил существенные количественные различия при сравнении контрольной и исследуемой групп (рис. 8.2.).
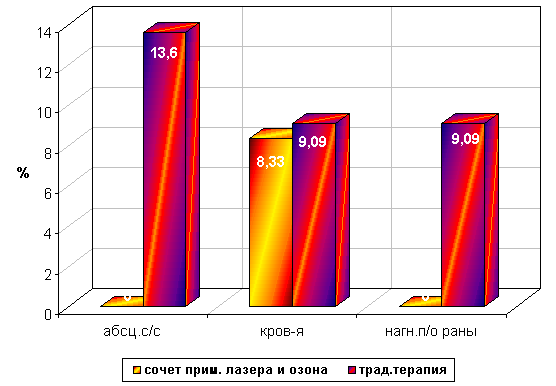
Рисунок 8.2. Сравнительная частота развития п/о осложнений у больных контрольной и исследуемой групп.
Из представленной диаграммы видно, что при сочетанном применении лазеро- и озонотерапии количество осложнений уменьшилось на 23,5%.
Таким образом, эффективность корригирующей антиоксидантной терапии у больных с панкреонекрозом подтверждается более ранней нормализацией клинико-лабораторных показателей, снижением частоты развития осложнений, уменьшением числа повторных операций и снижением летальности, которая в исследуемой группе больных составила 16,6%, что на 10,7% ниже, чем в контрольной группе.
Литература
Influence of correct antioxidant therapy on the microcirculation in pancreonecrosis
Y.S.Vinnik, D.V.Cherdancev, О.V.Pervova
The Krasnoyarsk state medical academy
The last years investigations proved presence the existence of direct correlation between the microcirculate disturbance degree and weight of pathological symptoms of oxidizing stress under acute necrotizing pancreatitis.
In the clinic of general surgery department was investigated the efficiency of the developed antioxidant therapy original method, which is based on combination of through skin infrared laser therapy and intravenous injection of the ozone physiological solution on microcirculation with 22 patients with the different forms of pancreonecrosis.
Results of our investigations showed, that on a background of correct antioxidant therapy, with the system activation of glutathione antioxidant system the improvement of peripheral microcirculation, reduction of frequency development destruction of pancreas, of frequency of development postoperations of purulent complications, reduction of number repeated operations and decrease mortality.